随着“临床试验数据自查核查”和“仿制药质量和疗效一致性评价”等政策的出台,临床试验的关注度不断提高。
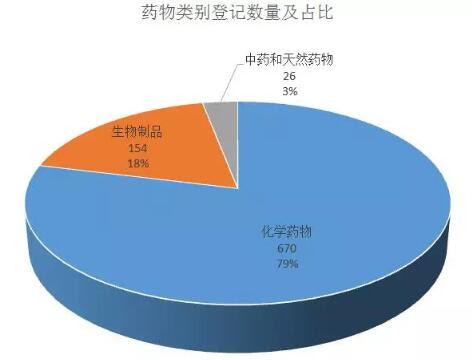
2018上半年,CDE药物临床试验登记平台总共公示880个临床试验。其中,化学药物670个,生物制品154个,中药/天然药物26个。
药物类别
国内试验和国际多中心试验
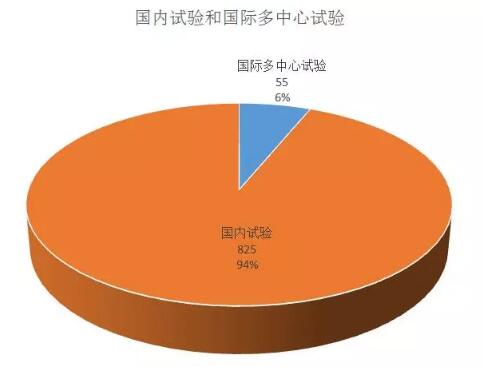
目前药物临床试验平台中的临床试验多以国内试验为主,2018年上半年总计55个国际多中心试验,54个都是2期和3期试验,主要研究安全性和有效性。从药品来看,55个均为新药临床试验。国际多中心试验中除百济神州的BGB-A317注射液外,试验数量较多的均为外企的临床试验研究。
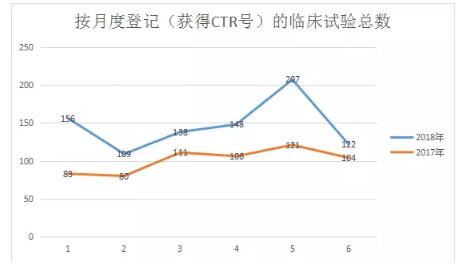
按月度登记(获得CTR号)的临床试验总数
临床试验登记数量来看,2018年上半年同比增加较多,其中5月更是达到了207个临床试验。
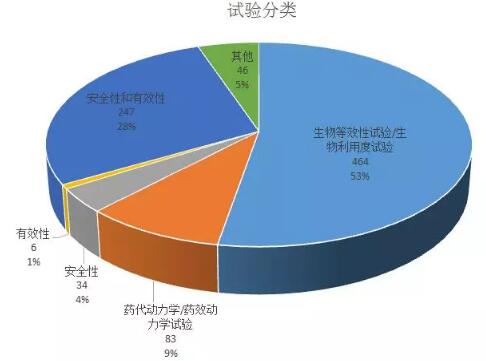
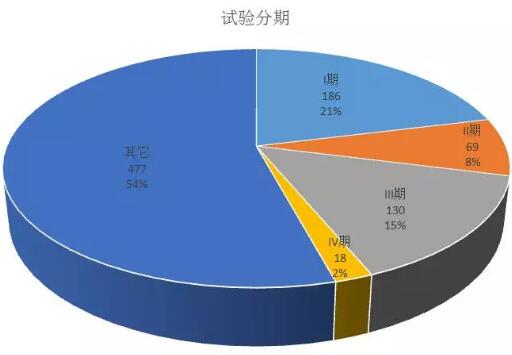
试验分类和分期,大家看看就好了,我这里就不做太多分析,主要是因为一致性评价的开展,和常规临床试验登记规律有一定不同。
试验分类
试验分期
2018上半年临床试验最受关注的药品TOP10
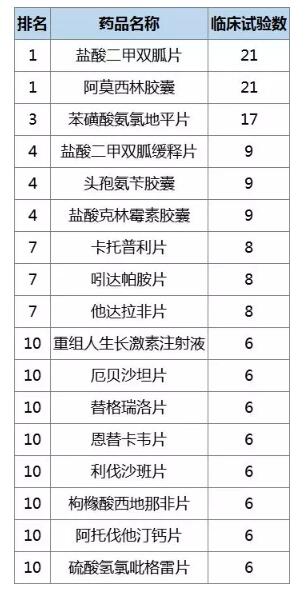
对药品的临床试验登记情况统计发现,2018上半年最受关注的药品为盐酸二甲双胍片和阿莫西林胶囊,其次是苯磺酸氨氯地平片。进一步分析发现,最受关注的药品TOP10共计158个试验,其中149个试验类型为生物等效性试验,占比94.3%。
表1:最受关注的临床试验药物TOP10
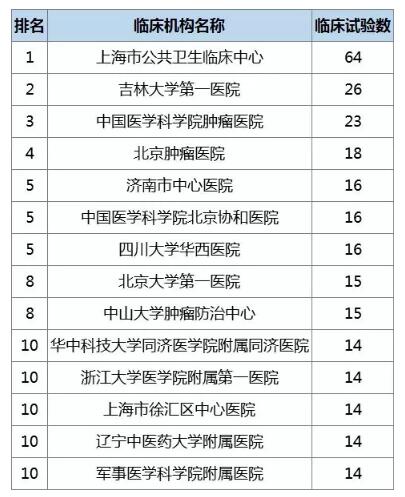
最忙碌的临床试验机构
最后简单看一下2018上半年最忙碌的临床试验机构,开展试验最多的是上海市公共卫生临床中心。我还是觉得国家应该建立一批专业的临床试验机构,独立于医院。另外,对于医院医生开展临床试验要有一些政策倾斜,比如职称评定等。
综上所述:纵观2018上半年已公示的临床试验,可以发现生物等效性试验所占比重较大,专业的临床试验机构承接的临床试验较多。本文数据来源于CDE药物临床试验登记与公示平台和药智中国临床试验数据库。
以上就是临床试验机构-桐晖药业小编分享的来自“药智网”有关“2018国内临床试验年中报告”的全部内容,供大家参考!
广州市桐晖药业有限公司是一家符合现代化管理要求的GSP公司,在进口原料药细分领域是为业界翘楚,为客户提供专业的从药学研发、临床预BE到临床BE的药厂研发一站式解决方案。目前的重点业务主要包括:原料药联合申报、参比制剂一次性进口、临床预BE/正式BE和一致性评价服务。如需合作,欢迎来电咨询!