2月20日,国家药品监督管理局药品审评中心(CDE)下发通知,对第一批拟不推荐参比制剂化药品种药学研究技术要求进行意见征求。这些品种因为临床价值明确,且无法推荐参比制剂,一致性评价应该是可以从简处理,按规定进行药学研究而不进行生物等效性试验。

《通知》显示,根据化学仿制药一致性评价工作相关要求,为促进仿制药质量提升,在《临床价值明确,无法推荐参比制剂的化学药品目录(第一批)》(征求意见稿)的基础上,CDE组织起草了《第一批拟不推荐参比制剂化药品种药学研究技术要求》(征求意见稿),经专家会讨论,目前已完成30个品种的药学研究技术要求,现在中心网站予以公示,以广泛听取各界意见和建议,欢迎各界提出宝贵意见和建议,并请及时反馈给CDE。征求意见时限为:2021年2月20日-2021年3月5日(10个工作日)。
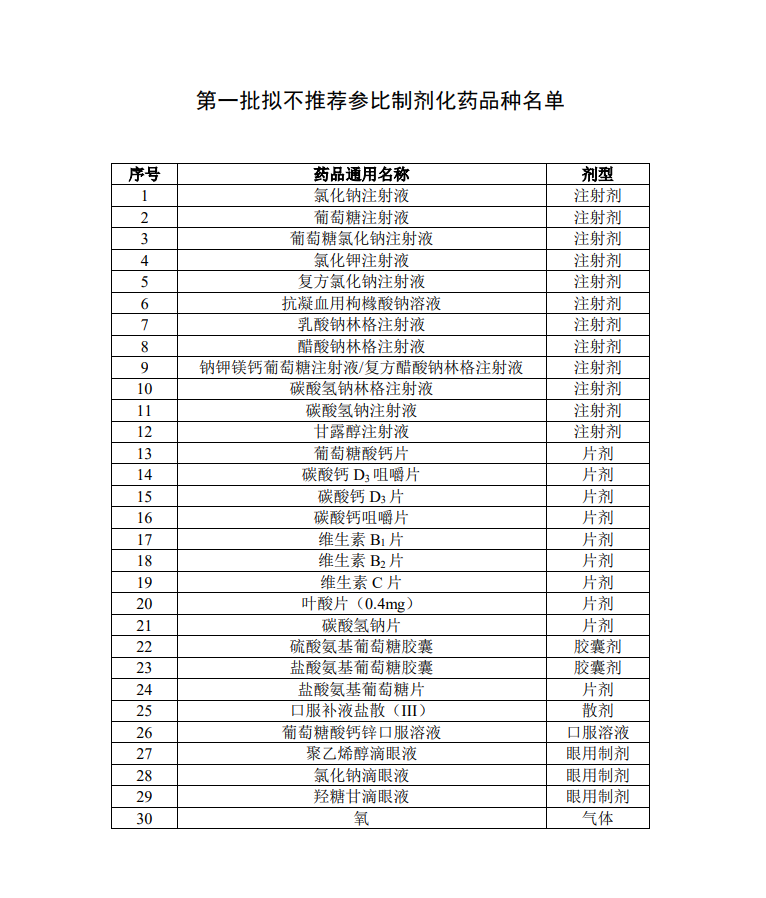
意见稿有7个附件为30个临床价值明确,无法推荐参比制剂的化学药的药学研究技术要求提供指导,包含氯化钠、葡萄糖等临床大规模、广泛应用的化学药品,其中包括12个注射剂、14个口服制剂、3个滴眼液、一个气体(氧气)。